วัคซีนเจอี (JE Vaccine)
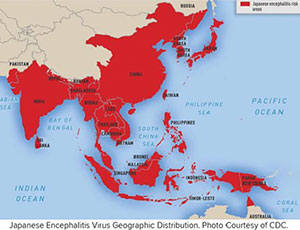
โรคไข้สมองอักเสบเจอี (Japanese Encephalitis) เป็นโรคที่เกิดจากไวรัสซึ่งแพร่โดยยุง โดยมีหมูและนกน้ำเป็นแหล่งรังโรค โรคนี้พบครั้งแรกในประเทศญี่ปุ่นช่วงปลายศตวรรษที่ 19 ปัจจุบันยังมีระบาดประปรายในแถบเอเชียแปซิฟิก
ยุงที่เป็นพาหะของโรคมักวางไข่ตามทุ่งนาและแหล่งน้ำขังในเขตชนบทหรือชานเมือง ผู้ติดเชื้อส่วนใหญ่มักไม่มีอาการ มีเพียงร้อยละ 0.1-1 เท่านั้นที่จะแสดงอาการของโรคไข้สมองอักเสบ และหากป่วยจะมีอัตราการเสียชีวิตสูง แม้ผู้รอดชีวิตก็อาจมีภาวะพิการทางระบบประสาท เนื่องจากผู้ใหญ่ส่วนใหญ่มีภูมิคุ้มกันแล้ว เด็กจึงเป็นกลุ่มเป้าหมายสำคัญของการให้วัคซีนป้องกัน
📖 ประวัติการพัฒนาวัคซีน
ไวรัส JE ถูกแยกได้ครั้งแรกในปี ค.ศ. 1935 วัคซีนเริ่มพัฒนาในญี่ปุ่นและจีนช่วงกลางศตวรรษที่ 20 โดยเริ่มจากวัคซีนเชื้อตายที่ผลิตจากสมองลูกหนู เรียกว่า MBD (Mouse brain-derived inactivated vaccine) วัคซีนนี้มีประสิทธิภาพสูง (97.5%) แต่มีผลข้างเคียงมาก จึงเลิกใช้ในเวลาต่อมา
วัคซีนรุ่นที่สอง ผลิตจากสายพันธุ์ Beijing-3 โดยเพาะในเซลล์ไตของหนูแฮมสเตอร์และฆ่าเชื้อด้วย propiolactone ทำให้บริสุทธิ์ด้วย column chromatography ใช้ชื่อการค้าว่า JEVAC® ผลิตโดยบริษัท Chengda Biotechnology (จีน)
วัคซีนรุ่นที่สาม ใช้สายพันธุ์ SA-14-14-2 เพาะใน Vero cell และฆ่าเชื้อด้วยฟอร์มาลิน ผลิตโดยบริษัท Intercell ในนาม IXIARO® ได้รับการขึ้นทะเบียนในยุโรป อเมริกา แคนาดา ออสเตรเลีย และประเทศอื่น ๆ อีกมาก
วัคซีนรุ่นที่สี่ เป็นวัคซีนเชื้อเป็นแต่ทำให้อ่อนฤทธิ์ ใช้เชื้อสายพันธุ์ SA-14-14-2 เพาะผ่านเซลล์หนูแฮมสเตอร์มากกว่า 100 ครั้ง ผลิตโดย Chengdu Institute of Biological Products ใช้ชื่อการค้าว่า CD.JEVAX® ฉีดเข้าใต้ผิวหนัง (subcutaneous) มีใช้ในไทยอย่างแพร่หลาย
วัคซีนรุ่นที่ห้า ใช้เทคโนโลยีพันธุวิศวกรรม โดยนำยีนส์ PrM และ E ของไวรัสเจอีสายพันธุ์ SA-14-14-2 ใส่แทนยีนส์เดียวกันของไวรัสไข้เหลืองสายพันธุ์ 17D ผลิตเป็นวัคซีนไวรัสผสม (chimeric virus vaccine) โดยบริษัท Sanofi Pasteur ใช้ชื่อการค้าว่า IMOJEV® ปัจจุบันมีใช้ในไทย
แม้จะมีชื่อทางการค้าอื่น ๆ เกิดขึ้นมากมาย แต่ยังใช้หลักการและสายพันธุ์ไวรัสตามที่กล่าวมาข้างต้น วัคซีนทุกชนิดต้องเก็บไว้ที่อุณหภูมิ 2-8°C และห้ามแช่แข็ง อายุการเก็บรักษาโดยทั่วไปอยู่ที่ 1-3 ปี
🏥 การใช้ในประเทศไทย
ประเทศไทยเริ่มฉีดวัคซีนเจอีชนิดเชื้อตายในแผนวัคซีนพื้นฐานตั้งแต่ปี พ.ศ. 2533 และเปลี่ยนเป็นชนิดเชื้อเป็นอ่อนฤทธิ์ในปี 2543 ซึ่งมีประสิทธิภาพและความปลอดภัยมากกว่า
ปัจจุบันองค์การเภสัชกรรมไทยสามารถผลิตวัคซีนเจอีได้ เด็กไทยทุกคนจะได้รับฟรี โดยเริ่มฉีดเข็มแรกที่อายุ 9-12 เดือน และเข็มที่สองเมื่ออายุ 2 ปี หากมีข้อห้ามสำหรับวัคซีนเชื้อเป็น จึงพิจารณาใช้วัคซีนเชื้อตายแทน
ในนักท่องเที่ยวที่พำนักในไทยนานเกิน 4 สัปดาห์ โดยเฉพาะผู้ที่เดินทางไปยังชนบทหรือใกล้ฟาร์มหมู ควรประเมินความเสี่ยงและอาจพิจารณาฉีดวัคซีนเชื้อตาย เช่น JEVAC® หรือ IXIARO® โดยฉีด 2 เข็มห่างกัน 7-28 วัน
⏏ ภูมิคุ้มกันที่เกิดขึ้น
วัคซีนเชื้อตาย IXIARO® ก่อภูมิคุ้มกันได้ 98% หลังฉีดครบ และยังคงมีภูมิถึง 83% หลัง 1 ปี ส่วน JEVAC® สามารถสร้างภูมิได้ 100% เมื่อฉีดครบ
วัคซีนเชื้อเป็น CD.JEVAX® ก่อภูมิได้ 100% และยังคงอยู่ถึง 96.5% หลัง 5 ปี ส่วน IMOJEV® ก่อภูมิในเด็ก 96% และในผู้ใหญ่ 99.1%
⚠️ ผลข้างเคียงที่อาจพบ
IXIARO® อาจมีอาการแดง บวม ปวดบริเวณฉีด (ไม่เกิน 1%) ปวดศีรษะ (26%) ปวดกล้ามเนื้อ (21%) อ่อนเพลียและคล้ายหวัด (13%)
JEVAC® อาการปวดบริเวณฉีดน้อยกว่า 4% มีไข้ไม่เกิน 18% ส่วนใหญ่มักเกิดในเข็มแรกภายใน 1-2 วัน
CD.JEVAX® อาการแดง บวม หรือปวดบริเวณฉีดน้อยกว่า 3% อาจมีไข้ อาเจียน ปวดกล้ามเนื้อ หรือผื่นตามตัวน้อยกว่า 9%
IMOJEV® ในผู้ใหญ่ อาการเจ็บบริเวณฉีด 12.4% แดง 4.6% คัน 4% ปวดศีรษะ 26% อ่อนเพลีย 22.8% ปวดกล้ามเนื้อ 16.6% ในเด็ก อาการเจ็บ 32% แดง 23% บวม 9% ไข้ 21% งอแง 28% เบื่ออาหาร 26% อาเจียน 20% ง่วงซึม 18% อาการเหล่านี้ไม่แตกต่างจากกลุ่มที่ได้วัคซีนหลอกหรือวัคซีนไวรัสตับอักเสบเอ
จากการศึกษาระยะที่ 4 ในอาสาสมัคร 10,000 ราย พบว่าวัคซีน IMOJEV® มีความปลอดภัยสูง
📌 สรุป
- โรคไข้สมองอักเสบเจอีเกิดจากไวรัสที่ยุงเป็นพาหะ มีแหล่งรังโรคคือหมูและนกน้ำ
- วัคซีนพัฒนาแล้วหลายรุ่น มีทั้งแบบเชื้อตาย เชื้อเป็น และวัคซีนพันธุวิศวกรรม
- ประเทศไทยใช้วัคซีนนี้ในแผนพื้นฐาน โดยฉีดฟรีในเด็กเล็กทุกคน
- ภูมิคุ้มกันจากวัคซีนหลายชนิดมีประสิทธิภาพดี ยาวนาน และปลอดภัย
- ผลข้างเคียงที่พบส่วนใหญ่ไม่รุนแรง และคล้ายกับวัคซีนทั่วไป
บรรณานุกรม
- Marc Fischer, et al. 2010. "Japanese Encephalitis Vaccines: Recommendations of the Advisory Committee on Immunization Practices (ACIP)." [ระบบออนไลน์]. แหล่งที่มา CDC. (3 พฤษภาคม 2564).
- Nagendra R. Hegde and Milind M. Gore. 2017. "Japanese encephalitis vaccines: Immunogenicity, protective efficacy, effectiveness, and impact on the burden of disease." [ระบบออนไลน์]. แหล่งที่มา Hum Vaccin Immunother. 2017;13(6):1320–1337. (3 พฤษภาคม 2564).
- Vijaya Satchidanandam. 2020. "Japanese Encephalitis Vaccines." [ระบบออนไลน์]. แหล่งที่มา Curr Treat Options Infect Dis. 2020;12:1–12. (5 พฤษภาคม 2564).
- Scott Kitchener. "The rise and fall of Japanese Encephalitis vaccination in the ADF – Where to now?" [ระบบออนไลน์]. แหล่งที่มา JMVH.Org. (3 พฤษภาคม 2564).
- Kriengsak Limkittikul. "Japanese encephalitis and vaccines." [ระบบออนไลน์]. แหล่งที่มา Dept Trop Ped, Mahidol University. (3 พฤษภาคม 2564).
- "Japanese encephalitis vaccine." [ระบบออนไลน์]. แหล่งที่มา Wikipedia. (3 พฤษภาคม 2564).
- "ตำราวัคซีนและการสร้างเสริมภูมิคุ้มกันโรค." [ระบบออนไลน์]. แหล่งที่มา กระทรวงสาธารณสุข. (21 เมษายน 2564).
- "ตารางการให้วัคซีนในเด็กไทย." [ระบบออนไลน์]. แหล่งที่มา สมาคมโรคติดเชื้อในเด็กแห่งประเทศไทย. (20 เมษายน 2564).