ขั้นตอนการวิจัยและผลิตยา
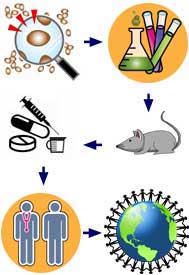 ยาแผนปัจจุบันมีที่มาจากการศึกษากลไกการเกิดโรค โดยมุ่งทำความเข้าใจว่าสารเคมีหรือกระบวนการใดในร่างกายมีบทบาทต่อการดำเนินโรค และมีสารชนิดใดที่สามารถกระตุ้นหรือยับยั้งกระบวนการเหล่านั้นให้สวนทางกับการเกิดโรคได้ การพัฒนายาใหม่แต่ละชนิดจึงเป็นกระบวนการที่ซับซ้อนและใช้เวลายาวนานนับสิบปี เริ่มต้นจากการคัดเลือกสารสำคัญที่มีศักยภาพเป็นยา จากสารประกอบจำนวนกว่าหมื่นชนิด เพื่อนำมาศึกษาความแรงในการออกฤทธิ์และความเป็นพิษในระดับหลอดทดลอง จากนั้นจึงทดสอบการเปลี่ยนแปลงของยาในสัตว์ทดลอง เพื่อประเมินการกระจายตัวของยา ปริมาณที่ก่อให้เกิดพิษ รวมถึงความเสี่ยงในการก่อมะเร็ง
ยาแผนปัจจุบันมีที่มาจากการศึกษากลไกการเกิดโรค โดยมุ่งทำความเข้าใจว่าสารเคมีหรือกระบวนการใดในร่างกายมีบทบาทต่อการดำเนินโรค และมีสารชนิดใดที่สามารถกระตุ้นหรือยับยั้งกระบวนการเหล่านั้นให้สวนทางกับการเกิดโรคได้ การพัฒนายาใหม่แต่ละชนิดจึงเป็นกระบวนการที่ซับซ้อนและใช้เวลายาวนานนับสิบปี เริ่มต้นจากการคัดเลือกสารสำคัญที่มีศักยภาพเป็นยา จากสารประกอบจำนวนกว่าหมื่นชนิด เพื่อนำมาศึกษาความแรงในการออกฤทธิ์และความเป็นพิษในระดับหลอดทดลอง จากนั้นจึงทดสอบการเปลี่ยนแปลงของยาในสัตว์ทดลอง เพื่อประเมินการกระจายตัวของยา ปริมาณที่ก่อให้เกิดพิษ รวมถึงความเสี่ยงในการก่อมะเร็ง
เมื่อผ่านขั้นตอนดังกล่าวแล้ว จึงเข้าสู่การพัฒนารูปแบบยาและกำหนดขนาดยาที่เหมาะสม เพื่อให้ยามีความคงตัว สามารถออกฤทธิ์ได้อย่างมีประสิทธิภาพ และรองรับการผลิตในระดับอุตสาหกรรม ขั้นตอนถัดมาคือการทดสอบประสิทธิภาพและความปลอดภัยของยาในมนุษย์ ซึ่งเป็นกระบวนการสำคัญในการยืนยันว่ายาสามารถใช้รักษาโรคได้จริงและปลอดภัยต่อผู้ใช้ หลังจากยาผ่านการขึ้นทะเบียนและออกจำหน่ายแล้ว ยังต้องมีการติดตามความปลอดภัยของผู้ป่วยอย่างต่อเนื่อง เพื่อยืนยันประสิทธิผลของยาในข้อบ่งใช้ที่ได้รับอนุมัติ และเฝ้าระวังอาการไม่พึงประสงค์ในระยะยาว
การศึกษาวิจัยยาในมนุษย์
ขั้นตอนที่ต้องอาศัยความระมัดระวังสูงสุดคือการวิจัยยาทางคลินิก (Clinical trials) ซึ่งเป็นการศึกษาการเปลี่ยนแปลงของยาในร่างกายมนุษย์ โดยครอบคลุมการดูดซึมของยา การกระจายตัวในอวัยวะต่าง ๆ ระดับความเข้มข้นของยาในเลือดตามช่วงเวลาหลังรับยา การเปลี่ยนแปลงโครงสร้างทางเคมีของยา การขับถ่ายออกจากร่างกาย ตลอดจนการประเมินผลการรักษาและอาการไม่พึงประสงค์ที่อาจเกิดขึ้น เวชภัณฑ์ทุกชนิดที่ขึ้นทะเบียนเป็นยาแผนปัจจุบันจำเป็นต้องผ่านกระบวนการนี้ และต้องยื่นขออนุญาตต่อคณะกรรมการพิจารณาการศึกษาวิจัยในมนุษย์ และสำนักงานคณะกรรมการอาหารและยา กระทรวงสาธารณสุขของประเทศที่ทำการศึกษา ก่อนเริ่มการวิจัยทุกครั้ง
ในหลายกรณี การวิจัยยาจำเป็นต้องรวบรวมอาสาสมัครจากหลายประเทศ โดยเฉพาะโรคที่พบไม่บ่อยหรือมีคุณสมบัติเฉพาะ เพื่อให้ได้จำนวนตัวอย่างเพียงพอสำหรับการวิเคราะห์ทางสถิติ การดำเนินการดังกล่าวต้องขออนุมัติจากหน่วยงานกำกับดูแลของทุกประเทศที่เข้าร่วม และต้องอาศัยทีมบุคลากรทางการแพทย์และวิจัยที่มีความเชี่ยวชาญ รวมถึงเจ้าหน้าที่ที่สามารถสื่อสารด้วยภาษาท้องถิ่นของผู้เข้าร่วมการศึกษา
การวิจัยยาทางคลินิกแบ่งออกเป็น 4 ระยะ ได้แก่
- ระยะศึกษาด้านความปลอดภัย เป็นการศึกษาการใช้ยาชนิดใหม่ในมนุษย์เป็นครั้งแรก โดยอาจทำในอาสาสมัครที่มีสุขภาพดีหรือผู้ป่วยโรคนั้น ๆ จำนวนประมาณ 20–100 คน เพื่อประเมินการดูดซึมของยา ความสัมพันธ์ระหว่างขนาดยากับระดับยาในร่างกาย การเปลี่ยนแปลงของยา กลไกและระยะเวลาในการออกฤทธิ์ รวมถึงขนาดต่ำสุดที่ให้ผลการรักษา และอาการไม่พึงประสงค์ที่อาจเกิดขึ้นจากขนาดยาที่แตกต่างกัน
ระยะเวลาการศึกษาในระยะนี้อาจกินเวลาหลายเดือน โดยมีเพียงประมาณร้อยละ 70 ของการวิจัยที่สามารถผ่านระยะนี้ได้ ซึ่งหมายความว่ายานั้น มีความปลอดภัยในการใช้ในมนุษย์ และ ทราบขนาดยาที่เหมาะสม
- ระยะศึกษาประสิทธิภาพของยา การวิจัยในระยะนี้จะทำเฉพาะยาที่ผ่านการศึกษาในระยะที่ 1 แล้ว โดยทำการศึกษาในผู้ป่วยที่มีโรคหรือภาวะตามข้อบ่งใช้ จำนวนประมาณ 100–300 คน เพื่อประเมินประสิทธิภาพของยาในการรักษา พร้อมติดตามอาการไม่พึงประสงค์ในระยะสั้นจากการใช้ยาในขนาดที่เหมาะสม
การศึกษาในระยะที่สองใช้เวลาตั้งแต่หลายเดือนจนถึงประมาณ 2 ปี และมีเพียงร้อยละ 30 เท่านั้นที่สามารถผ่านไปได้ โดยต้องได้ผลว่า ยามีประสิทธิภาพในการรักษาโรคนั้น และ ทราบผลข้างเคียงในขนาดที่ใช้รักษา
- ระยะทดลองใหญ่ เป็นการศึกษาที่ทำเฉพาะยาที่ผ่านการวิจัยระยะที่ 2 แล้ว โดยจะทดลองในผู้ป่วยประมาณ 300–3,000 ราย พร้อมกันในสถานพยาบาลหลายแห่ง มีการเปรียบเทียบกับกลุ่มควบคุมที่ได้รับยาหลอกหรือการรักษามาตรฐานเดิม เพื่อประเมินความสมดุลระหว่างประโยชน์ ความเสี่ยง และอาการไม่พึงประสงค์ที่พบได้น้อยหรือเกิดขึ้นในระยะยาว
การศึกษาในระยะนี้ใช้เวลาประมาณ 1–4 ปี และมีเพียงร้อยละ 25 ที่สามารถผ่านระยะนี้ได้ โดยต้องแสดงให้เห็นว่า ยามีประสิทธิผลเทียบเท่าหรือดีกว่าวิธีรักษาเดิม และ มีข้อมูลผลข้างเคียงที่ชัดเจนและละเอียดขึ้น
ยาที่ผ่านการวิจัยในระยะที่สามแล้วสามารถยื่นขอขึ้นทะเบียนยาเพื่อจำหน่ายในท้องตลาดได้ แต่หลังจากได้รับอนุมัติแล้ว ยังจำเป็นต้องมีการศึกษาและติดตามข้อมูลต่อไปในระยะที่ 4
- ระยะตรวจติดตามหลังการวางจำหน่าย เป็นการเฝ้าระวังความปลอดภัยของผู้ป่วยภายหลังยาถูกนำออกใช้ในวงกว้าง เพื่อยืนยันประสิทธิผลของยาในข้อบ่งใช้ที่ได้รับอนุมัติ และรวบรวมข้อมูลอาการไม่พึงประสงค์ในระยะยาว หากพบว่ายามีผลข้างเคียงรุนแรงเกินกว่าประโยชน์ที่ได้รับ อาจต้องเพิกถอนยาออกจากท้องตลาด หรือปรับปรุงคำเตือนและวิธีการใช้เพื่อเพิ่มความปลอดภัย
บริษัทที่คิดค้นและพัฒนายาใหม่จนผ่านการศึกษาทางคลินิกระยะที่ 3 สามารถจดทะเบียนสิทธิบัตรยา เพื่อเป็นผู้ผลิตและจัดจำหน่ายยาแต่เพียงผู้เดียว โดยในประเทศไทย สิทธิบัตรยามีอายุคุ้มครองสูงสุด 20 ปี ในช่วงเวลานี้ บริษัทอื่นไม่สามารถผลิตยาชื่อสามัญที่มีสูตรตำรับและคุณสมบัติทางเคมีเหมือนกับยาต้นแบบได้ ยาใหม่ในระยะแรกจึงมักมีราคาสูง เพื่อชดเชยค่าใช้จ่ายในการวิจัยและพัฒนาที่ใช้เวลายาวนาน
เมื่อสิทธิบัตรสิ้นสุดลง บริษัทยาอื่นสามารถผลิตยาชื่อสามัญออกจำหน่ายได้ การแข่งขันในตลาดช่วยให้ราคายาลดลง การขึ้นทะเบียนยาชื่อสามัญไม่จำเป็นต้องมีข้อมูลการศึกษาระยะก่อนทดลองในมนุษย์หรือการวิจัยทางคลินิกระยะที่ 1–3 แต่ต้องมีการศึกษาเปรียบเทียบการดูดซึมและการออกฤทธิ์ เพื่อยืนยันว่ามีประสิทธิภาพและความปลอดภัยไม่แตกต่างจากยาต้นแบบ ยาชื่อสามัญจึงใช้เวลาและงบประมาณในการพัฒนาน้อยกว่า ช่วยเพิ่มทางเลือกในการรักษาให้ประชาชน ลดภาระค่าใช้จ่ายด้านสาธารณสุข และลดการพึ่งพาการนำเข้ายาราคาสูงจากต่างประเทศ
กระบวนการผลิตยา
การผลิตยาเพื่อจำหน่ายในทุกประเทศทั่วโลกจำเป็นต้องเป็นไปตามหลักเกณฑ์วิธีการที่ดีในการผลิตยา (Good Manufacturing Practice, GMP) ขององค์การอนามัยโลก เพื่อประกันคุณภาพ ความปลอดภัย และความสม่ำเสมอของยาทุกรุ่นก่อนถึงมือผู้บริโภค
การผลิตยาแต่ละรูปแบบมีกระบวนการที่แตกต่างกันดังนี้
 การผลิตยาเม็ด
การผลิตยาเม็ด
กระบวนการผลิตยาเม็ดเริ่มจากการเตรียมและผสมวัตถุดิบตัวยาสำคัญเข้ากับสารช่วยต่าง ๆ จากนั้นเติมสารยึดเกาะ เพื่อให้ได้ผงแกรนูล ซึ่งเป็นกลุ่มของผงยาที่จับตัวกันเป็นก้อนเล็ก ๆ ผงแกรนูลนี้จะถูกทำให้แห้งด้วยความร้อน หรือกระแสลมร้อน ก่อนนำไปตอกอัดเป็นเม็ดยา
ในบางกรณี เม็ดยาอาจต้องผ่านกระบวนการเคลือบด้วยน้ำตาลหรือฟิล์ม เพื่อป้องกันการเสื่อมสภาพของตัวยาสำคัญ กลบรสหรือกลิ่นที่ไม่พึงประสงค์ หรือควบคุมให้ยาไปออกฤทธิ์ในตำแหน่งที่ต้องการ เช่น ลำไส้ เมื่อสิ้นสุดกระบวนการผลิตแล้ว จะต้องมีการสุ่มตัวอย่างยาเพื่อนำไปตรวจวิเคราะห์คุณภาพ ปริมาณตัวยาสำคัญในแต่ละเม็ด และตรวจสอบการปนเปื้อนก่อนบรรจุจำหน่าย
 การผลิตยาแคปซูล
การผลิตยาแคปซูล
แคปซูลทำหน้าที่เสมือนภาชนะที่บรรจุตัวยาอยู่ภายใน และสามารถรับประทานได้ เนื่องจากผลิตจากโปรตีนชนิดหนึ่ง ที่เรียกว่าเจลาติน แคปซูลแบ่งออกเป็น 2 ชนิด ได้แก่
- แคปซูลแข็ง ประกอบด้วยส่วนตัวแคปซูลและฝาปิด โดยตัวยาที่ผ่านการเตรียมในรูปผงหรือผงแกรนูล จะถูกบรรจุลงในตัวแคปซูล แล้วจึงนำฝาปิดมาประกบเข้าด้วยกัน ตัวอย่างเช่น แคปซูลยาปฏิชีวนะ
- แคปซูลนิ่ม เป็นแคปซูลที่ผลิตเปลือกและบรรจุตัวยาไปพร้อมกัน ทำให้มีลักษณะขอบปิดสนิท น้ำและอากาศไม่สามารถซึมผ่านได้ ตัวอย่างเช่น แคปซูลน้ำมันตับปลา ก่อนนำไปบรรจุจำหน่าย แคปซูลต้องผ่านกระบวนการขัดเพื่อลดการปนเปื้อนของฝุ่นผงยา และผ่านการตรวจวิเคราะห์คุณภาพและปริมาณตัวยาสำคัญเช่นเดียวกับยาเม็ด
 การผลิตยาน้ำ
การผลิตยาน้ำ
ยาน้ำแบ่งออกเป็น 2 ชนิด คือ
- ยาน้ำเนื้อเดียว เป็นสารละลายที่มีลักษณะเป็นเนื้อเดียวกันทั้งขวด กระบวนการผลิตเริ่มจากการละลายตัวยาในตัวทำละลาย และกวนให้กระจายตัวอย่างสม่ำเสมอ ในบางกรณีอาจใช้ความร้อนช่วยในการละลาย หากตัวยาสำคัญไม่เสื่อมสภาพจากความร้อน จากนั้นจึงเติมสารอื่น ๆ เช่น สารแต่งสี กลิ่น รส และสารกันเสีย
- ยาน้ำเนื้อผสม ได้แก่
- อิมัลชั่น (Emulsions) เป็นส่วนผสมระหว่างของเหลวประเภทน้ำมัน (Oil Phase) กับตัวยาที่ละลายในน้ำ (Aqueous Phase) โดยมีสารช่วยประสานให้ของเหลวทั้งสองเข้ากันได้ เรียกว่าอิมัลซิไฟเออร์ (Emulsifiers) ตัวอย่างเช่น วิตามิน A&D ไซรัป
- ยาแขวนตะกอน (Suspension) เป็นยาที่มีตัวยาอยู่ในรูปของแข็ง ไม่ละลายน้ำ แต่แขวนลอยอยู่ในน้ำกระสายยา โดยมีสารช่วยพยุงตัวยา เช่น กลีเซอรีนไกลคอล เพื่อให้ตัวยากระจายตัวได้สม่ำเสมอ เมื่อเขย่าขวดก่อนใช้ จะช่วยให้ยามีความเข้มข้นเท่ากันทั่วทั้งขวด
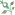 การผลิตยากึ่งของแข็ง
การผลิตยากึ่งของแข็ง
ยากึ่งของแข็ง ได้แก่ ครีม ขี้ผึ้ง โลชั่น เจล และยาทาภายนอก
มีกระบวนการผลิตคล้ายกับการผลิตยาอิมัลชั่น แต่จะมีการเติมสารเพิ่มความหนืด สารลดแรงตึงผิว และสารช่วยการดูดซึมผ่านผิวหนังเข้าไปด้วย จากนั้นนำส่วนผสมเข้าเครื่องปั่นจนได้เนื้อเดียวกัน
สำหรับขี้ผึ้ง จะมีการผสมพาราฟินเพื่อให้ได้ลักษณะกึ่งแข็ง ส่วนครีม โลชั่น และเจล มักมีการเติมสารแต่งกลิ่นเพิ่มเติม หากไม่รบกวนต่อความคงตัวและฤทธิ์ของตัวยาสำคัญ
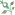 การผลิตยาปราศจากเชื้อ
การผลิตยาปราศจากเชื้อ
ยาปราศจากเชื้อคือยาที่เตรียมขึ้นให้ปราศจากเชื้อจุลินทรีย์ทุกชนิด
และมีฤทธิ์ในการรักษาโรค เช่น ยาฉีด และยาหยอดตา
เนื่องจากต้องใช้มาตรฐานการควบคุมที่เข้มงวดเป็นพิเศษ
ยากลุ่มนี้จึงมักมีราคาสูงกว่ายารับประทานทั่วไป
การผลิตยาปราศจากเชื้อต้องเริ่มจากการคัดเลือกวัตถุดิบที่มีคุณภาพสูง
และควบคุมทุกขั้นตอนการเตรียมยาในสภาพแวดล้อมที่สะอาด
เพื่อป้องกันการปนเปื้อนของเชื้อจุลินทรีย์ ฝุ่นละออง
และสิ่งแปลกปลอมที่อาจก่อให้เกิดอาการไม่พึงประสงค์
เช่น ไข้หรือหนาวสั่นหลังการใช้ยา
เมื่อบรรจุยาแล้ว จะต้องผ่านการอบฆ่าเชื้อด้วยไอน้ำอีกครั้ง
เพื่อประกันคุณภาพและความปลอดภัยก่อนนำไปใช้
ยาฉีดถือเป็นรูปแบบยาที่มีความซับซ้อนเป็นพิเศษ
นอกจากตัวยาสำคัญแล้ว ยังอาจมีสารอื่นประกอบอยู่ด้วย
เช่น สารช่วยละลายตัวยา (Cosolubilizers)
สารช่วยเพิ่มความคงตัวทางกายภาพและทางเคมี
สารกันเสียเพื่อคงสภาพการปราศจากเชื้อ
รวมถึงสารที่ช่วยลดความเจ็บปวดหรือการระคายเคืองขณะฉีดยา
สิ่งสำคัญในการให้กำเนิดยา
แม้ในปัจจุบันจะมีกระแสตั้งคำถามและคัดค้านการใช้ยาเพื่อเร่งรัด
หรือแทรกแซงกระบวนการเยียวยาตามธรรมชาติของร่างกายเพิ่มมากขึ้น
โดยเฉพาะในประเทศที่เป็นแหล่งวิจัยและผลิตยาเอง
แต่ก็ไม่อาจปฏิเสธได้ว่ายายังคงมีบทบาทสำคัญต่อการดำรงชีวิตของมนุษยชาติ
สิ่งสำคัญคือ การลงทุนคิดค้นและผลิตยาแต่ละชนิด
ไม่ควรมุ่งหวังผลทางการตลาดมากเกินไป
ไม่เร่งผลักดันให้ยาต้อง “ผ่าน” ทุกขั้นตอนการวิจัยด้วยกลไกทางสถิติ
และไม่โหมโฆษณาให้ผู้คนใช้ยาก่อนความจำเป็น
มิฉะนั้น การให้กำเนิดยาที่ต้องอาศัยเวลาและเงินลงทุนต่อเนื่องยาวนานกว่าสิบปี
อาจกลายเป็นการให้กำเนิดปัจจัยที่บั่นทอนสมดุลของระบบนิเวศทางธรรมชาติ
และระบบสุขภาพของสังคมในระยะยาวได้
สรุป
ยาแผนปัจจุบันเป็นผลลัพธ์ของกระบวนการวิจัยและพัฒนาที่ซับซ้อน ใช้เวลายาวนาน และต้องอาศัยความรู้ทางวิทยาศาสตร์ เทคโนโลยี และจริยธรรมในระดับสูง ตั้งแต่การศึกษากลไกการเกิดโรค การคัดเลือกสารที่มีศักยภาพเป็นยา การทดสอบในระดับหลอดทดลองและสัตว์ทดลอง ไปจนถึงการวิจัยยาทางคลินิกในมนุษย์ซึ่งแบ่งออกเป็น 4 ระยะ
เพื่อยืนยันทั้งประสิทธิภาพ ความปลอดภัย และความคุ้มค่าในการนำไปใช้รักษาโรคจริง
เมื่อยาผ่านการวิจัยจนได้รับอนุมัติให้จำหน่ายแล้ว กระบวนการผลิตยาทุกขั้นตอนต้องเป็นไปตามหลักเกณฑ์ วิธีการที่ดีในการผลิตยา (GMP) เพื่อควบคุมคุณภาพ ความปลอดภัย และความสม่ำเสมอของยาในทุกรุ่น โดยรูปแบบยาที่แตกต่างกัน เช่น ยาเม็ด แคปซูล ยาน้ำ ยากึ่งของแข็ง และยาปราศจากเชื้อ ต่างก็มีขั้นตอนการผลิตเฉพาะที่เหมาะสมกับลักษณะการใช้งานและความต้องการทางการรักษา
แม้ยาจะมีบทบาทสำคัญต่อการดูแลสุขภาพของมนุษยชาติ แต่การให้กำเนิดยาหนึ่งชนิดต้องอาศัยการตัดสินใจอย่างรอบคอบ ไม่ควรถูกขับเคลื่อนด้วยแรงจูงใจทางการตลาดเพียงอย่างเดียว การพัฒนายาที่มีคุณภาพ ปลอดภัย และใช้เท่าที่จำเป็น ไม่เพียงช่วยรักษาผู้ป่วยรายบุคคล แต่ยังเป็นการรักษาสมดุลของระบบสุขภาพ สังคม และสิ่งแวดล้อมในระยะยาวอีกด้วย