ยาปฏิชีวนะ (Antibiotics)
ยาปฏิชีวนะเป็นยากลุ่มหนึ่งในบรรดายาต้านจุลชีพ ซึ่งออกฤทธิ์จำเพาะต่อเชื้อแบคทีเรียเป็นหลัก ยาบางชนิดอาจครอบคลุมเชื้อริกเค็ทเซีย คลาไมเดีย และแบคทีเรียชั้นสูงบางกลุ่มได้ด้วย อย่างไรก็ตาม ยาปฏิชีวนะ ไม่ออกฤทธิ์ต่อเชื้อไวรัส จึงไม่มีประโยชน์ในการนำมาใช้รักษาโรคติดเชื้อไวรัส เช่น ไข้หวัดใหญ่ ไข้เลือดออก หัด อีสุกอีใส คางทูม เป็นต้น คำว่า “ยาฆ่าเชื้อ” ที่ใช้เรียกกันทั่วไปในชีวิตประจำวันจึงอาจทำให้เกิดความเข้าใจคลาดเคลื่อนได้
ยาปฏิชีวนะสามารถจำแนกออกเป็นกลุ่มต่าง ๆ ได้หลายแนวทาง ดังนี้
- จำแนกตามลักษณะการออกฤทธิ์ แบ่งเป็นยาที่ออกฤทธิ์ฆ่าเชื้อแบคทีเรียโดยตรง (Bactericidal antibiotics) และยาที่ออกฤทธิ์เพียงยับยั้งการเจริญเติบโตของเชื้อ (Bacteriostatic antibiotics) โดยอาศัยระบบภูมิคุ้มกันของร่างกายช่วยกำจัดเชื้อในขั้นต่อไป
- จำแนกตามการใช้งานทางคลินิก แบ่งเป็นยาที่ออกฤทธิ์ครอบคลุมเชื้อแบคทีเรียหลายกลุ่ม (Broad-spectrum antibiotics) และยาที่ออกฤทธิ์จำเพาะต่อเชื้อเพียงบางกลุ่ม (Narrow-spectrum antibiotics)
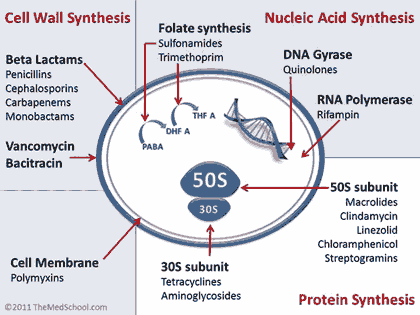
- จำแนกตามกลไกทางเภสัชวิทยา โดยพิจารณาจากกลไกที่ยาใช้ทำอันตรายต่อเชื้อ เช่น การยับยั้งการสร้างผนังเซลล์ การยับยั้งการสังเคราะห์กรดนิวคลิอิก หรือการยับยั้งการสร้างโปรตีน นอกจากนี้ ยาที่ออกฤทธิ์ในกลไกเดียวกันยังสามารถแบ่งย่อยออกตามโครงสร้างทางเคมีได้อีกหลายกลุ่ม ตัวอย่างเช่น ยากลุ่ม β-lactams ซึ่งมีโครงสร้าง β-lactam ring เป็นองค์ประกอบสำคัญ ส่วนชื่อกลุ่มยาที่ลงท้ายด้วยตัวอักษร -s มักสะท้อนว่ายังมียาอนุพันธ์อีกหลายชนิดที่พัฒนาต่อยอดจากโครงสร้างตั้งต้นเดียวกัน
กลไกการดื้อยาของเชื้อแบคทีเรีย
การที่แบคทีเรียไม่ตอบสนองต่อยาปฏิชีวนะอาจเกิดขึ้นได้ตั้งแต่โดยธรรมชาติ ตัวอย่างเช่น แบคทีเรียแกรมลบส่วนใหญ่ไม่ไวต่อยาเพนิซิลลิน แม้ว่าจะต้องมีการสร้างผนังเซลล์เช่นเดียวกัน ขณะที่แบคทีเรียแกรมบวกจำนวนมากไม่ตอบสนองต่อยากลุ่มอะมิโนกลัยโคไซด์ ทั้งที่ต่างก็ต้องอาศัยการสังเคราะห์โปรตีนภายในเซลล์ กลไกการดื้อยาโดยกำเนิดนี้เป็นหนึ่งในเหตุผลสำคัญที่ทำให้ต้องมีการพัฒนายาต้านเชื้อจุลชีพหลากหลายกลุ่ม เพื่อให้สามารถรักษาโรคติดเชื้อจากแบคทีเรียชนิดต่าง ๆ ได้อย่างเหมาะสม
นอกจากการดื้อยาโดยธรรมชาติแล้ว แบคทีเรียยังสามารถพัฒนาการดื้อยาขึ้นใหม่ได้จากการปรับตัว เมื่อได้รับยาปฏิชีวนะซ้ำ ๆ แต่ไม่ถูกทำลายอย่างสมบูรณ์ กลไกการดื้อยาที่เกิดจากการปรับตัวนี้ ปัจจุบันพบว่ามีอยู่ 5 วิธีหลัก ได้แก่
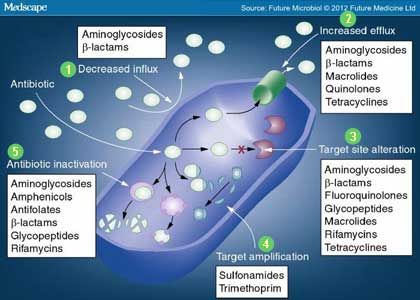
- ลดการผ่านเข้าสู่เซลล์ของยา (Decreased influx)
- เร่งการขับยาออกจากเซลล์ (Increased efflux)
- เปลี่ยนแปลงตำแหน่งเป้าหมายของยา (Target site alteration)
- เพิ่มจำนวนหรือสร้างเป้าหมายใหม่ของยา เพื่อทดแทนตำแหน่งที่ถูกยาจับไว้ (Target amplification)
- ทำลายยาปฏิชีวนะโดยตรง (Antibiotic inactivation) เช่น การสร้างเอนไซม์ขึ้นมาทำลายโครงสร้างของยา
แบคทีเรียหนึ่งตัวสามารถมีกลไกดื้อยาได้มากกว่าหนึ่งวิธีพร้อมกัน ส่งผลให้เกิดภาวะดื้อยาหลายขนาน (multidrug resistance) ซึ่งเป็นปัญหาที่ร้ายแรงอย่างยิ่ง โดยเฉพาะในผู้ป่วยที่ติดเชื้อซึ่งมียาที่ใช้รักษาได้จำกัด หากเชื้อดื้อยาทั้งหมด ผู้ป่วยจะมีทางเลือกในการรักษาน้อยมากและมีความเสี่ยงต่อการเสียชีวิตสูง
ยิ่งไปกว่านั้น กลไกการดื้อยาดังกล่าวยังสามารถถ่ายทอดสู่รุ่นถัดไปของแบคทีเรียเองได้ (Vertical gene transfer) และยังสามารถถ่ายทอดข้ามสายพันธุ์ไปยังแบคทีเรียชนิดอื่น (Horizontal gene transfer) 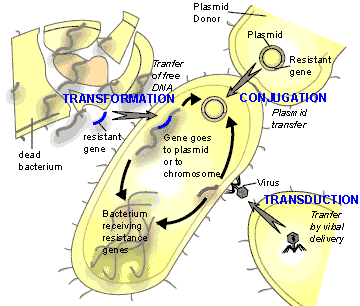 ซึ่งปัจจุบันพบว่ามีกลไกหลัก 3 วิธี ได้แก่
ซึ่งปัจจุบันพบว่ามีกลไกหลัก 3 วิธี ได้แก่
1. Conjugation เกิดขึ้นเมื่อแบคทีเรียสองตัวอยู่ใกล้กันและสามารถถ่ายทอดชิ้นส่วนดีเอ็นเอ หรือ plasmids ให้แก่กันได้ ถือเป็นวิธีการถ่ายทอดยีนที่สำคัญที่สุด
2. Transformation เป็นกระบวนการที่แบคทีเรียมีชีวิตรับเอาชิ้นส่วนดีเอ็นเอจากซากของแบคทีเรียที่ตายแล้วในสิ่งแวดล้อมเข้าสู่เซลล์ของตน
3. Transduction เป็นการถ่ายทอดดีเอ็นเอของแบคทีเรียจากตัวหนึ่งไปสู่อีกตัวหนึ่งโดยอาศัยไวรัสที่ติดเชื้อแบคทีเรีย (bacteriophages) เป็นตัวกลาง
พัฒนาการของยาปฏิขีวนะกลุ่มต่าง ๆ
การพัฒนายาปฏิชีวนะมีความสัมพันธ์อย่างใกล้ชิดกับปัญหาโรคติดเชื้อในแต่ละยุคสมัย รวมถึงการเกิดและการแพร่กระจายของเชื้อแบคทีเรียดื้อยา
- ยุคบุกเบิก: Sulfonamides
ซัลโฟนาไมด์ถือเป็นยาปฏิชีวนะเชิงพาณิชย์กลุ่มแรกของโลก เริ่มจากการพัฒนา Prontosil ในช่วงต้นทศวรรษที่ 1930 ยากลุ่มนี้ออกฤทธิ์แบบ bacteriostatic โดยยับยั้งการสังเคราะห์กรดโฟลิกซึ่งจำเป็นต่อการเจริญและแบ่งตัวของแบคทีเรีย แม้จะช่วยลดอัตราการเสียชีวิตจากการติดเชื้อได้อย่างมากในยุคแรก แต่ปัจจุบันบทบาทลดลงเนื่องจากการดื้อยาและผลข้างเคียง
- ปลายทศวรรษ 1930: กำเนิด β-lactams
การค้นพบเพนิซิลลินโดย Alexander Fleming และการผลิตในระดับอุตสาหกรรมในช่วงปลายทศวรรษ 1930 เปิดฉากยุคทองของยาปฏิชีวนะ ยากลุ่ม β-lactams ออกฤทธิ์ยับยั้งการสร้างผนังเซลล์แบคทีเรีย ทำให้เชื้อแตกและตาย มีความปลอดภัยสูงและกลายเป็นรากฐานสำคัญของการรักษาโรคติดเชื้อ ต่อมามีการพัฒนาอนุพันธ์ต่าง ๆ เช่น cephalosporins, carbapenems และ monobactams
- ทศวรรษ 1940-1950: ยาที่ออกฤทธิ์ยับยั้งการสังเคราะห์โปรตีนที่หน่วยย่อย 30S ของไรโบโซม
- Aminoglycosides เช่น streptomycin มีบทบาทสำคัญในการรักษาวัณโรคและการติดเชื้อแกรมลบรุนแรง ออกฤทธิ์แบบ bactericidal แต่มีข้อจำกัดด้านพิษต่อไตและประสาทหู
- Tetracyclines เป็นยากลุ่ม broad-spectrum ครอบคลุมเชื้อแกรมบวก แกรมลบ และเชื้อ atypical แม้ได้รับความนิยมสูงในอดีต แต่ปัจจุบันบทบาทลดลงจากปัญหาการดื้อยา
- Chloramphenicol เคยมีบทบาทมากในประเทศกำลังพัฒนาเนื่องจากราคาถูก แต่การเกิดภาวะกดไขกระดูกและ aplastic anemia ทำให้การใช้งานถูกจำกัดอย่างมาก
- Macrolides เช่น erythromycin พัฒนาขึ้นเพื่อใช้ในผู้ป่วยที่แพ้เพนิซิลลิน โดยเฉพาะการติดเชื้อทางเดินหายใจและเชื้อ atypical และยังคงมีบทบาทสำคัญในเวชปฏิบัติปัจจุบัน
- ทศวรรษ 1960: ยาสำรองและการรับมือเชื้อดื้อยา
- Glycopeptides เช่น vancomycin ใช้รักษาการติดเชื้อแกรมบวกดื้อยา โดยเฉพาะ MRSA ออกฤทธิ์ยับยั้งการสร้างผนังเซลล์ในตำแหน่งที่แตกต่างจาก β-lactams จึงมักใช้เป็นยาทางเลือกสุดท้าย
- Ansamycins โดยเฉพาะ rifampicin มีบทบาทสำคัญในการรักษาวัณโรคและโรคติดเชื้อเรื้อรัง ออกฤทธิ์ยับยั้งการสังเคราะห์ RNA ของแบคทีเรีย
- ทศวรรษ 1970: ยาปฏิชีวนะสังเคราะห์เต็มรูปแบบ
Quinolones และ Fluoroquinolones เป็นยาปฏิชีวนะสังเคราะห์ที่ออกฤทธิ์ต่อเอนไซม์ DNA gyrase และ topoisomerase IV ทำให้การจำลองดีเอ็นเอของแบคทีเรียหยุดชะงัก ยากลุ่มนี้มีประสิทธิภาพสูง แต่มีแนวโน้มเกิดการดื้อยาได้รวดเร็ว
- ทศวรรษ 1980 - ปัจจุบัน: ยุคของยาขั้นสูงและยาสำรอง
- Oxazolidinones เช่น linezolid ใช้รักษาเชื้อแกรมบวกดื้อยาหลายชนิด โดยออกฤทธิ์ยับยั้งขั้นตอนเริ่มต้นของการสังเคราะห์โปรตีน
- Streptogramins เป็นการใช้ยาสองชนิดร่วมกันเพื่อเสริมฤทธิ์กัน มีบทบาทในการรักษาเชื้อแกรมบวกดื้อยารุนแรง
- Lipopeptides เช่น daptomycin ออกฤทธิ์ทำลายเยื่อหุ้มเซลล์แบคทีเรียโดยตรง มีประสิทธิภาพสูงและพบการดื้อยาน้อย
สรุป
ยาปฏิชีวนะเป็นเครื่องมือสำคัญในการรักษาโรคติดเชื้อแบคทีเรีย แต่มีขอบเขตการใช้งานที่ชัดเจนและไม่สามารถใช้รักษาโรคติดเชื้อไวรัสได้ การเข้าใจชนิดของยา กลไกการออกฤทธิ์ และข้อจำกัดของแต่ละกลุ่มมีความสำคัญต่อการเลือกใช้ยาอย่างเหมาะสม ขณะเดียวกัน การดื้อยาของเชื้อแบคทีเรียซึ่งเกิดได้ทั้งโดยธรรมชาติและจากการปรับตัว เป็นปัญหาสาธารณสุขระดับโลกที่ทวีความรุนแรงขึ้น การใช้ยาปฏิชีวนะอย่างสมเหตุสมผลและมีความรับผิดชอบจึงเป็นหัวใจสำคัญในการชะลอการเกิดเชื้อดื้อยา และคงประสิทธิภาพของยากลุ่มนี้ไว้สำหรับการรักษาผู้ป่วยในอนาคต