มะเร็งไขกระดูก (Multiple myeloma หรือ Plasmacytoma)
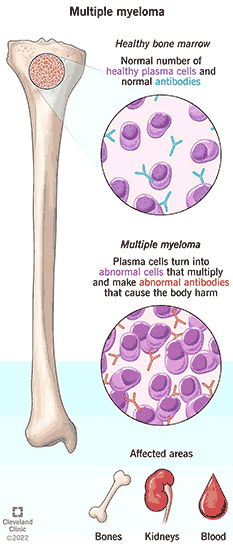
Multiple myeloma (MM) เป็นมะเร็งที่เกิดจากการเพิ่มจำนวนของ เซลล์พลาสมา (plasma cell) ชนิดโคลนเดียวในไขกระดูก โดยเซลล์มะเร็งเหล่านี้จะสะสมในกระดูกและก่อตัวเป็นก้อนมะเร็ง มักพบในกระดูกสันหลัง กระดูกอก และซี่โครง ส่วนที่พบอยู่นอกกระดูกพบได้น้อย เช่น เนื้อเยื่อรอบกระดูกสันหลัง เนื้อเยื่อบริเวณใบหน้า กล่องเสียง โพรงจมูก หรือเนื้อเยื่อใต้ผิวหนัง มะเร็งไขกระดูกพบประมาณ 15% ของมะเร็งทางโลหิตวิทยาทั้งหมด และมักพบในผู้ที่มีอายุเฉลี่ย 55 ปีขึ้นไป ทั้งเพศชายและเพศหญิง
เซลล์พลาสมาเป็นเม็ดเลือดขาวชนิดหนึ่งในไขกระดูก มีหน้าที่สร้างแอนติบอดีหรืออิมมูโนโกลบูลิน (Immunoglobulin) หลายชนิด โดยปกติในไขกระดูกจะมีเซลล์พลาสมาเพียง 2–3% แต่หากเกิดโรคจะพบปริมาณเกิน 10% ร่วมกับการสร้างโปรตีนผิดปกติในเลือด เรียกว่า เอ็มโปรตีน (M Protein – Monoclonal Protein) ซึ่งอาจเป็น IgG, IgA, Light chain κ/λ หรือชนิดหายากอื่น ๆ
อาการของโรค
กลุ่มอาการสำคัญ คือ CRAB: C = แคลเซียมในเลือดสูง, R = ไตเสื่อม, A = โลหิตจาง, B = รอยโรคทำลายกระดูก (bone lesions)
อาการที่พบบ่อย
- ปวดหลังหรือปวดกระดูกบ่อย กระดูกหักง่ายจากภาวะกระดูกพรุน
- อ่อนเพลีย เหนื่อยง่าย จากภาวะโลหิตจาง
- คลื่นไส้ สับสน จากระดับแคลเซียมในเลือดสูง
- ปัสสาวะเป็นฟอง บวม ขาบวม หรือมีครีเอตินีนสูงจากการทำงานของไตเสื่อม
- ติดเชื้อง่ายจากภูมิคุ้มกันที่บกพร่อง
- เสียงแหบหรือหายใจลำบาก หากก้อนอยู่ที่กล่องเสียงหรือทางเดินหายใจส่วนบน
- ชาที่มือหรือเท้า หรือเส้นประสาทอักเสบจากโรคหรือผลข้างเคียงของยา
เอกซเรย์กระดูกอาจพบรอยโรคทำลายกระดูกหลายตำแหน่ง (multiple osteolytic lesions) ตรงกับจุดที่มีอาการปวดหรือกระดูกหัก
การตรวจวินิจฉัย
- ตรวจเลือดและปัสสาวะ: CBC, ครีเอตินีน, แคลเซียม, อัลบูมิน, β2-microglobulin, LDH, โปรตีนในเลือดแบบแยกส่วน (SPEP/UPEP) ร่วมกับ immunofixation และตรวจ serum free light chains
- ตรวจไขกระดูก: ดูดหรือเจาะชิ้นเนื้อไขกระดูก เพื่อยืนยันว่ามีเซลล์พลาสมาชนิดโคลนิก ≥10% หรือพบพลาสมาไซโตมา พร้อมตรวจ FISH/NGS เพื่อประเมินความเสี่ยง
- ตรวจภาพถ่าย: แนะนำใช้ low-dose whole-body CT หรือ FDG-PET/CT หรือ whole-body MRI แทนการถ่ายฟิล์มโครงกระดูกแบบเดิม
- เกณฑ์วินิจฉัย (IMWG): ต้องพบ clonal plasma cell ร่วมกับ CRAB หรือ SLiM-CRAB ข้อใดข้อหนึ่ง
SLiM-CRAB (ตัวชี้วัดทางชีวภาพที่บ่งชี้ว่าเป็นมะเร็งแม้ยังไม่เกิดอวัยวะเสียหาย)
- S: สัดส่วนเซลล์พลาสมาในไขกระดูก ≥60%
- Li: อัตราส่วน free light chain (κ/λ) ผิดปกติอย่างมาก (involved/uninvolved ≥100 และ absolute ≥100 mg/L)
- M: MRI พบรอยโรคเฉพาะจุด ≥2 ตำแหน่ง
- ตรวจยีนผิดปกติ: เช่น del(17p), t(4;14), t(14;16), gain 1q, del 1p หรือมียีนกลายพันธุ์ TP53 จัดเป็นกลุ่มเสี่ยงสูง (high-risk) หากมี 2–3 ปัจจัยเรียกว่า double-/triple-hit
การรักษา
การรักษามะเร็งมัยอิโลมาพัฒนาเร็วมากในช่วงไม่กี่ปีที่ผ่านมา ทั้งสูตรยารุ่นใหม่ การปลูกถ่ายสเต็มเซลล์ การรักษาด้วย CAR-T และแอนติบอดีชนิดสองแขน (bispecific antibodies) โดยแนวทางจะเลือกตามอายุ ความแข็งแรงของผู้ป่วย ความรุนแรงของโรค และทรัพยากรที่มี
A. ยังไม่เข้าเกณฑ์มะเร็งไขกระดูก
หากพบก้อนมะเร็งมัยอิโลมาตำแหน่งเดียวโดยไม่มีอาการของมะเร็งไขกระดูก รักษาโดยฉายรังสีเฉพาะที่ ส่วนการผ่าตัดไม่แนะนำ ยกเว้นกรณีมีกระดูกสันหลังทรุดหรือแตกหักที่จำเป็นต้องเสริมความแข็งแรงของกระดูก
B. เข้าเกณฑ์มะเร็งไขกระดูก หรือพบก้อน 2 ตำแหน่งขึ้นไป
- Induction Chemotherapy:
- Quadruplet แนะนำ: daratumumab + bortezomib + lenalidomide + dexamethasone (Dara-VRd) เหมาะกับผู้ป่วยที่สามารถปลูกถ่ายได้ เพิ่มโอกาสการตอบสนองลึกและยืดระยะปลอดโรค
- ทางเลือก: VRd (สามยา) หรือสูตรอื่นปรับตามโรคร่วม/ข้อจำกัด
- ปลูกถ่ายสเต็มเซลล์ตนเอง (ASCT): ใช้กันแพร่หลายสำหรับผู้ป่วยที่เหมาะสม ช่วยยืดระยะควบคุมโรค
- ปลูกถ่ายสเต็มเซลล์ตนเอง (ASCT): ช่วยยืดการควบคุมโรคในผู้ป่วยที่เหมาะสม
- Maintenance:
- Lenalidomide เป็นมาตรฐาน โดยเฉพาะในผู้ป่วยกลุ่มเสี่ยงมาตรฐาน
- กลุ่มเสี่ยงสูงอาจใช้ร่วมกับ bortezomib ตามดุลยพินิจแพทย์
- การดูแลพยุงและป้องกันภาวะแทรกซ้อน:
- ให้ยากลุ่มกระดูก (bisphosphonate หรือ denosumab) พร้อมวิตามิน D/แคลเซียม
- ป้องกันเชื้อไวรัสเริม (เช่น acyclovir) เมื่อใช้ PI/แอนติบอดีบางชนิด
- ฉีดวัคซีนที่เหมาะสม เช่น ไข้หวัดใหญ่และ pneumococcus
- ดูแลอาการเฉียบพลัน เช่น แคลเซียมสูง ไตวาย เลือดหนืด กระดูกหักกดทับ
- การรักษากระดูกหัก: อาจใช้การฉายรังสี ผ่าตัดเสริมซีเมนต์ (cementoplasty) โดยเฉพาะที่กระดูกสันหลังจะทำ kyphoplasty ตามด้วย vertebroplasty หรือใช้รังสีตัด (radiofrequency ablation)
C. โรคกำเริบ/ดื้อยา (Relapsed/Refractory)
- สูตรยาใหม่: ผสมผสาน carfilzomib, pomalidomide, daratumumab/isatuximab, selinexor ตามประวัติการรักษา
- ภูมิคุ้มกันบำบัดขั้นสูง:
- CAR-T (BCMA-directed): ide-cel (Abecma) และ cilta-cel (Carvykti) ได้รับอนุมัติและมีแนวโน้มใช้เร็วขึ้นตามหลักฐานใหม่
- Bispecific antibodies: เช่น BCMAxCD3 (teclistamab, elranatamab, linvoseltamab) และ GPRC5D (talquetamab)
- Antibody-drug conjugates (ADC): belantamab mafodotin มีความคืบหน้าในหลายประเทศ แต่ในสหรัฐฯ อยู่ระหว่างการพิจารณาใหม่
การพยากรณ์โรค
อัตราการรอดชีวิตของผู้ป่วยเพิ่มขึ้นมากในช่วงทศวรรษที่ผ่านมา จากความก้าวหน้าของสูตรยา การปลูกถ่าย และภูมิคุ้มกันบำบัด อย่างไรก็ตาม MM ยังเป็นโรคเรื้อรังที่มีโอกาสกำเริบ จำเป็นต้องวางแผนการรักษาเป็นขั้นตอนและติดตามอย่างต่อเนื่อง ปัจจัยที่มีผลต่อการพยากรณ์ ได้แก่ อายุและสมรรถภาพ ระดับ β2-microglobulin และอัลบูมิน (ISS/R-ISS) ค่า LDH และความผิดปกติทางพันธุกรรม เช่น del(17p), gain 1q
สรุป
Multiple myeloma คือมะเร็งของเซลล์พลาสมาที่ก่อให้เกิดปัญหากลุ่มอาการ “CRAB” และมีตัวชี้วัด SLiM-CRAB เพื่อเริ่มรักษาก่อนเกิดอวัยวะเสียหาย การวินิจฉัยอาศัยผลเลือด-ปัสสาวะ ตรวจโปรตีนโมโนโคลนอล การตรวจไขกระดูก และการถ่ายภาพร่างกาย แนวทางรักษาเริ่มจากสูตร Dara-VRd ตามด้วยการปลูกถ่ายสเต็มเซลล์ (หากเหมาะสม) และ Maintenance ด้วย lenalidomide หากโรคกำเริบยังมีทางเลือกทรงพลัง เช่น CAR-T และ bispecific antibodies พยากรณ์โรคโดยรวมดีขึ้นมาก แต่ยังต้องติดตามระยะยาวและดูแลพยุงอย่างต่อเนื่อง